El Decreto 4725 de 2005 es una normativa esencial en Colombia que regula la comercialización, fabricación, distribución y vigilancia sanitaria de dispositivos médicos. Este decreto establece los lineamientos técnicos, sanitarios y administrativos que deben cumplirse para garantizar la calidad, seguridad y eficacia en el mantenimiento de los equipos biomédicos. En esta guía, profundizaremos en los aspectos fundamentales del decreto, la clasificación de los equipos, las responsabilidades de las instituciones y las estrategias que permiten un mantenimiento óptimo y seguro. Además, incluiremos enlaces de interés que te ayudarán a ampliar el conocimiento sobre temas complementarios, tales como el código GMDN, la Resolución 3100 y la implementación de programas de tecnovigilancia.
Contexto y Relevancia del Decreto 4725 de 2005
El Decreto 4725 de 2005 surge como respuesta a la necesidad de garantizar que todos los dispositivos médicos que se comercializan y utilizan en Colombia cumplan con rigurosos estándares de calidad y seguridad. Este marco regulatorio tiene como objetivo principal proteger la salud de los pacientes y asegurar que las instituciones de salud dispongan de equipos confiables para el diagnóstico y tratamiento.
Entre los objetivos principales del decreto se encuentran:
- Asegurar la seguridad de los pacientes y el personal de salud.
- Regular el uso adecuado de los dispositivos médicos.
- Establecer mecanismos de vigilancia y control sanitario.
Para una consulta directa del texto legal, puedes revisar el documento oficial publicado por el Ministerio de Salud en el siguiente enlace: Decreto 4725 de 2005 – Minsalud.
Clasificación de los Equipos Biomédicos
Una parte fundamental del decreto es la clasificación de los dispositivos médicos en función del nivel de riesgo. Los equipos se dividen en cuatro categorías:
Clase I (riesgo bajo),
Clase IIa (riesgo moderado),
Clase IIb (riesgo alto) y
Clase III (riesgo crítico). Esta clasificación es crucial para determinar los protocolos de mantenimiento y las medidas de seguridad que deben aplicarse.
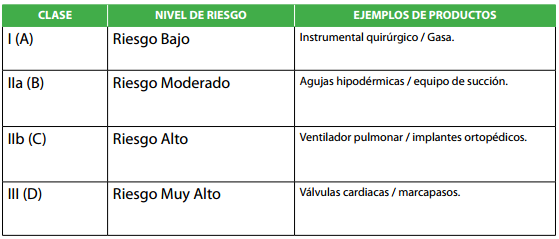
Por ejemplo, los dispositivos de Clase I incluyen productos como los guantes médicos, que presentan un riesgo mínimo, mientras que los de Clase III abarcan equipos críticos como desfibriladores e implantes, que requieren un mantenimiento muy riguroso.
Para entender de manera más profunda los criterios de clasificación y la identificación de dispositivos, te recomendamos leer nuestro artículo:
¿Qué es el código GMDN para dispositivos médicos?,
el cual explica cómo se codifican y clasifican los dispositivos a nivel internacional.
Asimismo, el INVIMA juega un papel importante en este proceso, ya que certifica y autoriza la comercialización de equipos biomédicos, garantizando que se cumplan los requisitos técnicos y de seguridad. Puedes consultar más sobre este tema en el siguiente enlace externo:
Dispositivos Médicos y Equipos Biomédicos – INVIMA.
Responsabilidades Institucionales en el Mantenimiento
El decreto establece que las instituciones de salud deben asumir responsabilidades claras en el mantenimiento de sus equipos biomédicos. Esto implica no solo la elaboración de programas de mantenimiento preventivo y correctivo, sino también la capacitación constante del personal técnico y la implementación de sistemas de seguimiento que permitan la trazabilidad de las intervenciones.
Entre las obligaciones institucionales destacan:
- Programas de mantenimiento: Las instituciones deben elaborar y ejecutar un programa que incluya inspecciones periódicas, calibraciones y procedimientos de limpieza.
- Capacitación del personal: Es fundamental que el personal técnico que interviene en el mantenimiento cuente con la formación necesaria. Para equipos clasificados como IIb y III, es imprescindible contar con el registro ante el INVIMA.
- Registros y documentación: Se debe llevar un historial detallado de cada intervención, con certificados de calibración y manuales de operación que aseguren la trazabilidad del mantenimiento.
Para profundizar en las normativas que complementan este proceso, consulta nuestro artículo sobre la Resolución 3100 y Dotación de Equipos Biomédicos en Colombia, el cual aborda aspectos regulatorios adicionales que impactan en el mantenimiento y la operatividad de estos dispositivos.
Sistemas de Gestión de Mantenimiento y Estrategias de Cumplimiento
Una herramienta esencial para cumplir con el decreto es la implementación de un Sistema de Gestión de Mantenimiento (CMMS). Estos sistemas permiten automatizar el seguimiento de las intervenciones, optimizar los tiempos de respuesta y garantizar la trazabilidad de cada acción.
Además, es recomendable:
- Realizar auditorías internas: Las auditorías permiten identificar posibles fallas en los protocolos de mantenimiento y aplicar mejoras continuas.
- Capacitar constantemente al personal: La formación continua es indispensable para asegurar que los técnicos estén actualizados en los procesos y normativas vigentes.
- Asociarse con proveedores certificados: Trabajar con proveedores reconocidos garantiza que los repuestos y servicios de soporte técnico cumplan con los estándares requeridos.
En este sentido, contar con un sistema automatizado no solo facilita la gestión, sino que también ayuda a minimizar los riesgos asociados a fallos en el equipo. El uso de herramientas tecnológicas es una estrategia clave para asegurar el cumplimiento normativo y mejorar la eficiencia operativa.
Vigilancia y Reporte de Eventos Adversos
El decreto establece la obligación de reportar cualquier evento adverso que se presente con los dispositivos médicos. Esta vigilancia es esencial para identificar y corregir posibles fallas que puedan comprometer la seguridad del paciente.
Entre las implicaciones prácticas de este punto se incluyen:
- Implementación de un sistema de monitoreo: Se debe contar con un mecanismo interno que permita la detección temprana de incidentes y la evaluación de su impacto.
- Análisis de causa raíz: Ante la ocurrencia de un evento adverso, es fundamental realizar un análisis exhaustivo que permita identificar las causas y establecer medidas correctivas.
- Reporte oportuno: La comunicación de eventos a las autoridades sanitarias, como el INVIMA, es una obligación que ayuda a mejorar la seguridad y a prevenir incidentes futuros.
Este enfoque proactivo en la vigilancia no solo cumple con lo estipulado en el decreto, sino que también fortalece la confianza en los procesos internos de la institución.

Documentación y Trazabilidad
Uno de los pilares del cumplimiento del Decreto 4725 es la adecuada documentación y la trazabilidad de todas las actividades relacionadas con el mantenimiento de los equipos biomédicos. La recopilación de datos y la conservación de historiales son fundamentales para demostrar que se han cumplido todos los protocolos establecidos.
Entre los documentos que deben mantenerse se encuentran:
- El registro sanitario del dispositivo.
- Los historiales de mantenimiento preventivo y correctivo.
- Los certificados de calibración (cuando aplica).
- El manual de operación y mantenimiento de cada equipo.
- Guías rápidas y protocolos internos de intervención.
Para conocer estrategias específicas de implementación, te recomendamos leer nuestra
Guía Práctica para Implementar tu Programa de Tecnovigilancia Relacionado con Equipos Biomédicos,
en la que se abordan técnicas para mejorar la documentación y la trazabilidad de los procesos de mantenimiento.
Importancia del Cumplimiento Normativo
El incumplimiento de las disposiciones del Decreto 4725 de 2005 puede acarrear sanciones administrativas y legales, además de poner en riesgo la seguridad de los pacientes. Por ello, cumplir con estas normativas es fundamental para:
- Reducir riesgos clínicos asociados a fallos de equipos.
- Aumentar la vida útil de los dispositivos biomédicos.
- Obtener acreditaciones y certificaciones de calidad en los servicios de salud.
- Fortalecer la confianza de pacientes y profesionales en el sistema de salud.
La correcta implementación de las normas también representa una ventaja competitiva para las instituciones, al demostrar un compromiso con la calidad y la seguridad.
Estrategias para Asegurar el Cumplimiento Normativo
Para lograr un mantenimiento efectivo y conforme a la normativa, se recomienda implementar diversas estrategias coordinadas. Algunas de estas estrategias incluyen:
- Uso de CMMS: Un sistema automatizado que permita planificar, ejecutar y documentar las intervenciones de mantenimiento.
- Capacitación continua: Programas de formación para el personal técnico, que garanticen competencias actualizadas y el cumplimiento de los requisitos del INVIMA.
- Auditorías internas periódicas: Revisiones constantes que permitan evaluar el cumplimiento de los protocolos y detectar áreas de mejora.
- Alianzas estratégicas con proveedores certificados: Trabajar con socios confiables que aseguren la calidad de los repuestos y el soporte técnico.
- Sistemas de tecnovigilancia: La implementación de un programa de tecnovigilancia ayuda a monitorear el desempeño de los equipos y a reportar cualquier evento adverso de manera oportuna.
Cada una de estas estrategias contribuye a la creación de un entorno seguro y eficiente en el mantenimiento de los equipos biomédicos, asegurando el cumplimiento de la normativa y minimizando los riesgos asociados.
Beneficios de una Gestión de Mantenimiento Eficiente
Adoptar un enfoque sistemático en el mantenimiento de equipos biomédicos ofrece múltiples beneficios para las instituciones de salud. Entre ellos se destacan:
- Mayor seguridad: Un mantenimiento riguroso reduce la probabilidad de fallos que puedan poner en riesgo la integridad de los pacientes y del personal médico.
- Optimización de recursos: La implementación de un CMMS permite un uso más eficiente de los recursos y una reducción en los tiempos de inactividad de los equipos.
- Mejora en la calidad del servicio: La confiabilidad de los equipos biomédicos se traduce en diagnósticos más precisos y en tratamientos más efectivos.
- Cumplimiento normativo: Garantizar la trazabilidad y la documentación adecuada ayuda a evitar sanciones legales y a mejorar la reputación de la institución.
Estos beneficios no solo impactan en la calidad de la atención médica, sino que también fortalecen la imagen institucional ante pacientes, proveedores y organismos reguladores.
Casos Prácticos y Ejemplos de Éxito
Numerosas instituciones han implementado exitosamente las recomendaciones del Decreto 4725 de 2005 mediante la adopción de sistemas de gestión integrados, la capacitación continua y la realización de auditorías internas. Estos casos de éxito demuestran que una buena gestión del mantenimiento puede marcar la diferencia en la operatividad y seguridad de los equipos biomédicos.
Por ejemplo, un hospital de gran envergadura implementó un sistema CMMS que le permitió reducir en un 30% el tiempo de respuesta ante fallos en sus equipos de diálisis (clasificados como Clase IIb), garantizando la continuidad del servicio y aumentando la satisfacción de los pacientes. Esta experiencia se complementó con la capacitación periódica del personal técnico, el uso de repuestos certificados y la implementación de un riguroso programa de tecnovigilancia.
Además, en instituciones donde se ha priorizado la documentación y la trazabilidad, se han logrado identificar rápidamente las causas de fallos recurrentes y se han implementado medidas correctivas que han prolongado la vida útil de los equipos, generando ahorros significativos y elevando los estándares de seguridad.
Recomendaciones Finales
El Decreto 4725 de 2005 representa un pilar fundamental para garantizar el mantenimiento seguro y eficiente de los equipos biomédicos en Colombia. La correcta aplicación de sus disposiciones implica no solo cumplir con la normativa, sino también implementar estrategias de gestión que fortalezcan la seguridad y la calidad en el sector salud.
Para lograr esto, es imprescindible:
- Elaborar programas de mantenimiento integrales y adaptados a la clasificación de cada equipo.
- Capacitar de manera continua al personal técnico, asegurando que cumpla con los requisitos del INVIMA.
- Implementar sistemas de gestión automatizados (CMMS) que faciliten la planificación y el seguimiento de las intervenciones.
- Realizar auditorías internas periódicas que permitan detectar oportunidades de mejora.
- Fomentar alianzas estratégicas con proveedores certificados y utilizar programas de tecnovigilancia para garantizar la trazabilidad de todas las acciones.
El cumplimiento normativo no solo evita sanciones administrativas y legales, sino que también protege la integridad de los pacientes y mejora la calidad del servicio de salud. Una gestión de mantenimiento bien estructurada es, en definitiva, una inversión en la seguridad y en la eficiencia operativa de cualquier institución.
En QS, nos especializamos en ayudar a las instituciones a implementar soluciones integrales que aseguren el cumplimiento de la normativa y optimicen el mantenimiento de equipos biomédicos. Si deseas conocer más sobre cómo podemos apoyarte en este proceso, no dudes en ponerte en contacto con nuestro equipo de expertos. ¡Construyamos juntos un sistema seguro y eficiente para tu institución!

Para ampliar tus conocimientos sobre normativas y regulaciones en el ámbito de los dispositivos médicos, te invitamos a revisar los siguientes recursos externos, los cuales aportan información complementaria y detallada:
- Consulta el
Decreto 4725 de 2005 en el sitio del Ministerio de Salud. - Revisa la información del INVIMA sobre
Dispositivos Médicos y Equipos Biomédicos.
Asimismo, complementa esta lectura con información interna que te permitirá entender otros aspectos críticos del sector:
- Aprende más sobre la
clasificación y el código GMDN para dispositivos médicos, que es esencial para identificar y clasificar los equipos según su nivel de riesgo. - Profundiza en la
Resolución 3100 y Dotación de Equipos Biomédicos en Colombia, la cual complementa las disposiciones del decreto. - Descubre nuestra Guía Práctica para Implementar tu Programa de Tecnovigilancia, fundamental para llevar un control riguroso de la seguridad y el mantenimiento.
En conclusión, el éxito en el mantenimiento de equipos biomédicos reside en la capacidad de combinar el cumplimiento normativo con la implementación de estrategias de gestión modernas y eficientes. Al aplicar las recomendaciones expuestas en este artículo, las instituciones de salud no solo aseguran la operatividad de sus equipos, sino que también fortalecen la confianza de sus pacientes y mejoran la calidad de los servicios prestados.
Adoptar un enfoque integral en el mantenimiento y la vigilancia de los dispositivos médicos es, sin duda, un desafío, pero también una oportunidad para optimizar recursos, garantizar la seguridad y posicionar a la institución como líder en calidad y eficiencia en el sector salud. La normativa vigente, junto con la implementación de tecnologías y procesos adecuados, forma la base para un sistema de mantenimiento robusto y confiable.
La transformación digital y la automatización de procesos, sumadas a una cultura de mejora continua y capacitación permanente, permitirán a las instituciones anticiparse a posibles fallos y responder de manera proactiva a cualquier eventualidad. De esta forma, se minimizan los riesgos y se garantiza que cada dispositivo biomédico funcione bajo los más altos estándares de seguridad, beneficiando tanto a los pacientes como a los profesionales de la salud.
Finalmente, recordar que la clave del éxito en el mantenimiento de equipos biomédicos es la coordinación entre la normativa, la tecnología y el factor humano. Sólo a través de un esfuerzo conjunto se podrá construir un sistema verdaderamente seguro y eficiente. En QS estamos comprometidos con este objetivo, brindándote las herramientas y el soporte necesario para que tu institución se destaque en el cumplimiento de la normativa y en la prestación de servicios de salud de alta calidad.
¡No esperes más! Ponte en contacto con nuestros expertos y descubre cómo transformar el mantenimiento de tus equipos biomédicos en un proceso seguro, eficiente y normativamente impecable.

